작은 유기 분자의 구조적 결정을 위한 X선, 전자 및 NMR 결정학
절뉴스 Vol.53 No.6
니시야마 유스케1, 2
1 (주)제올레조넌스 2 RIKEN CLST-JEOL 협업 센터
여기에서 우리는 RIKEN CLST-JEOL 공동 연구실에서 자연적으로 풍부한 저분자량 제약 화합물의 분자 구조를 탐구하기 위한 최근 개발을 발표합니다(동위원소 라벨링 없음). 고체 핵 자기 공명(ssNMR) 및 투과 전자 현미경(TEM)의 초고감도 카메라에서 빠른 매직 앵글 스피닝(MAS) 기술의 최근 발전은 제약 산업 및 과학의 문제에 답하는 새로운 방법을 제시합니다. 1) 결정 다형 및 2) 염/공결정은 품질 관리, 안정성 및 지적 재산 측면에서 두 가지 주요 관심사입니다. 결정 형태를 확인하기 위해 분말 X선 회절 및 13C 교차편광 MAS ssNMR은 널리 사용되는 방법이지만, 전자는 때때로 혼합물 분석에 적합하지 않으며 후자는 유사한 분자 구조를 가진 결정 형태를 구별하지 못합니다. 이러한 문제를 해결하기 위해 전자 회절(ED)과 1H 빠른 MAS NMR. 결정 형태는 ED를 사용하여 나노에서 마이크로미터 크기의 단결정에서 결정될 수 있는데, 이는 전자 상호작용이 X선 상호작용보다 4~5배 더 강하기 때문입니다. 1H NMR은 또한 분자 패킹에 적합한 정보를 제공합니다. 1H는 결정 표면에 있습니다. 수소가 중요한 역할을 하는 염/공결정 문제는 SCXRD(단결정 X선 회절)가 수소 원자 위치를 정확하게 결정할 수 없기 때문에 심각한 문제입니다. 여기서 우리는 사이의 핵간 거리를 결정합니다. 1H 및 15빠른 MAS 조건에서 ssNMR을 사용하는 N, 전체 구조는 SCXRD를 통해 얻어지며 염/공결정 질문에 답합니다.
개요
생명 공학 기반 의약품이 제약 시장에서 상위권에 나열되어 있지만 전통적인 저분자량 의약품은 여전히 성인병과 같은 일상적인 치료에 매우 중요합니다. 이러한 저분자량 활성 제약 성분(API)은 일반적으로 결정화 조건에 따라 여러 가지 다른 형태, 즉 결정 다형체로 결정화될 수 있습니다. 용해도와 안정성은 결정형의 영향을 많이 받기 때문에 개발 단계부터 생산 단계에 이르기까지 품질 관리 측면에서 결정형을 제어하고 모니터링하는 것이 매우 중요하다[1, 2, 3]. 충분히 큰 크기(~100μm)의 결정을 사용할 수 있는 경우 SCXRD(단결정 X선 회절)는 원자 분해능을 가진 결정 형태에 대한 뚜렷한 답을 제공합니다. 그러나 대부분의 저분자량 의약품은 정제, 환제, 산제 등 다양한 제형의 미정질 형태로 제공되고 있다. 이러한 제제는 부형제를 포함하므로 혼합물의 미세 결정에서 결정 형태를 결정하는 것이 중요합니다. 분말 X선 회절(PXRD) 및 13C 교차 편광 마법각 회전 핵 자기 공명(CPMAS NMR)은 결정 형태를 식별하는 두 가지 주요 방법입니다. 실험 패턴/스펙트럼은 각 결정 형태의 지문을 제공하므로 약물과 표준 형태 사이의 패턴/스펙트럼 비교는 대부분의 경우 그 안에 있는 결정에 대한 명확한 답을 제공합니다. 그러나 두 방법 모두 여전히 실질적인 문제가 있습니다. PXRD는 API와 부형제의 많은 회절 패턴이 서로 중첩되어 결정 형태를 식별하지 못하는 경우가 있습니다. 반면에, 13분자 형태에 민감한 C CPMAS는 대부분의 부형제 신호가 API 신호와 다른 위치에 나타나 신호가 중첩되는 것을 방지하기 때문에 혼합물 분석에 적합한 방법입니다. 하지만, 13C CPMAS는 탄소 원자가 분자 내부에 묻혀 있고 분자 표면에서 멀리 떨어져 있기 때문에 분자 패킹에 다소 둔감합니다. 그래서 13C CPMAS는 유사한 분자 구조를 가진 결정 형태를 식별하지 못합니다. 또한 결정 형태에 대한 민감도는 PXRD보다 낮습니다.
저분자량 API의 다른 주요 문제는 다성분 시스템에서 염/공결정/연속체를 식별하는 방법입니다. 때때로 API 결정의 용해도 및/또는 안정성을 개선해야 합니다. API와 비활성 코포머로 구성된 다성분 시스템은 이 문제에 대해 널리 사용되는 솔루션 중 하나입니다. (일반적으로 염기성) API와 (산성) 코포머를 혼합하여 다성분 시스템에서 많은 예를 찾을 수 있습니다. pKa(ΔpKa)의 차이가 3보다 크면 염이 형성되고 여기서 분자간 이온 상호작용이 발견됩니다. 소금에서 코포머의 양성자는 완전히 API 쪽으로 이동합니다. 최근에는 ΔpKa가 3 미만일 때 또 다른 종류의 다성분 시스템인 공결정이 도입됩니다. 공결정에서는 코포머의 양성자가 여전히 그곳에 머물며 분자간 수소 결합이 형성됩니다. 또한, 염과 공결정 사이의 시스템, 즉 양성자가 API와 코포머 사이에 위치하는 연속체도 발견됩니다. 특히 ΔpKa가 3보다 작은 경우 지적 관점에서 염/공결정/연속체를 식별하는 것이 중요합니다. 그러나 XRD 기반 방법에서 양성자 위치를 결정하는 능력의 부족은 염/공결정/ 연속체, 왜냐하면 그들 사이의 차이는 수소 위치에서만 오기 때문입니다.
아직 해결되지 않은 주요 문제는 1) 혼합물 분석, 2) 유사한 분자 구조를 가진 결정 형태 식별, 3) 결정 능력 부족입니다. 1H 위치. 앞의 두 가지 문제는 결정질 다형체와 관련이 있고 마지막 문제는 소금/공결정/연속체에 관한 것입니다. 여기에서 우리는 전자 회절(ED)을 결합합니다. 1H ssNMR 및 SCXRD는 이러한 문제를 해결합니다. ED는 TEM(Transmission Electron Microscopy) 장비의 관찰 방법 중 하나로 회절 패턴을 제공합니다. 전자의 상호작용이 X-ray보다 104~105배 강하기 때문에 나노에서 마이크로 크기의 단결정까지 ED 패턴을 관찰할 수 있어 혼합물 분석이 가능하다. ED의 적용은 주로 전자 조사에 강한 무기 물질에 국한되었지만 최근 고감도 카메라의 발전으로 극저온 시료 홀더와 함께 저선량 모드가 가능해 저분자량을 포함한 유기 결정의 ED 관찰이 가능해졌습니다. 무게 API. 문제 2)가 제기된 이유는 13C CPMAS는 위에서 언급한 바와 같이 분자 형태에 둔감합니다. 다행스럽게도 70kHz 이상의 매우 빠른 MAS 기술의 도입으로 고해상도가 가능해졌습니다. 1단단한 고체에서도 H 관찰 [4, 5, 6], 여기서 1H는 다음과 밀접하게 결합되어 있습니다. 1H-1적당한 MAS 속도에서 H 쌍극자 상호 작용. 부터 1H는 표면에 위치하며, 1H 등방성 화학적 이동은 형태뿐만 아니라 분자 패킹에도 민감합니다. 게다가, 1H-1H 분자간 상관 관계는 각 분자 패킹에 대해 뚜렷한 패턴을 제공합니다. Fast MAS 기술은 고해상도 뿐만 아니라 1H NMR뿐만 아니라 다음을 포함한 몇 가지 정교한 실험도 포함합니다. 14N NMR 및 1H-15N 거리 측정. 전자는 작은 유기 분자에서 양성자화된 상태를 나타냅니다. 후자는 수소 위치가 중요한 역할을 하는 염/공결정/연속체 문제에 대한 명확한 답을 제공합니다. 또한 각 방법의 처리량을 평가합니다.
결정 다형체[7]
제약 분야에서 결정 형태의 식별은 매우 중요하며 일반적으로 PXRD 및 13C CPMAS ssNMR. 그러나 전자는 혼합물 분석에 적합하지 않으며 후자는 위에서 설명한 것처럼 때때로 실패합니다. 예로서, 13L-히스티딘의 세 가지 다른 (유사) 다형체의 C CPMAS 스펙트럼이 그림 1에 나와 있습니다. L-히스티딘(그림 1b, c)은 L-히스티딘·HCl·H의 염산염과 뚜렷한 스펙트럼을 나타냅니다.2O (그림 1a), 분자 구조가 다르기 때문입니다. 한편, 사방정계(그림 1b)와 단사정계(그림 1c) 형태의 L-히스티딘은 거의 동일한 13서로 가까운 형태를 반영하는 C CPMAS 스펙트럼. 여기에 표시된 바와 같이, 13C CPMAS는 다른 형태의 결정형을 식별하는 민감한 측정법이지만 유사한 분자 형태를 가진 다형체를 구별하지 못합니다. 우리는 여기에서 ED와 1매우 빠른 MAS에서 H ssNMR을 사용하여 이러한 질문에 답하십시오.
그림 2는 L-histidine·HCl·H의 TEM 이미지와 ED 패턴을 보여준다.2O 실온에서 측정. 결정의 크기는 의약품에서 흔히 볼 수 있는 1μm 정도인데, 100nm 나노빔을 적용한다. 따라서 원칙적으로 100nm의 결정은 단결정 ED 패턴을 얻기에 충분히 큽니다. 실제로 우리는 100nm 또는 더 작은 결정에서 ED 패턴을 측정했습니다. L-histidine·HCl·H의 임계 용량으로2실온에서 O는 10-20e에 불과합니다.-nm-2, 선량률을 10e로 설정했습니다.-nm-2s-1 노출 시간 1초, 총 선량 10e-nm-2. 이러한 매우 낮은 선량 조건에서도 최첨단 CMOS 카메라(OneView, Gatan, Inc., USA)는 충분한 감도를 제공합니다. 10-20e의 임계 용량 동안-nm-2 일반적으로 유기 분자에서 발견되며 cryo 샘플 홀더는 필요한 경우 임계 선량을 추가로 향상시킵니다. ED 패턴은 결정 구조에서 쉽게 계산할 수 있으므로 실험과 계산된 ED 패턴을 비교하여 결정 형태를 식별할 수 있습니다. 사방정계 및 단사정계 형태의 L-히스티딘의 ED 패턴은 각각 그림 3과 그림 4에 나와 있습니다. 하는 동안 13C CPMAS는 이 두 가지 형태를 구별하지 못하며(그림 1), ED 회절은 각 결정 형태에 대해 뚜렷한 패턴을 제공합니다. 이는 이 두 가지 형태에서 격자 매개변수가 완전히 다르기 때문입니다. 또한 ED는 PXRD(수십 분)에 비해 XNUMX분 이내에 높은 처리량 측정이 가능하고 13C CPMAS(시간). ED 측정은 JEM-ARM200F(JEOL Ltd., Japan)를 사용하여 수행하였다. 대부분의 TEM 장비는 고감도 카메라가 설치된 경우 이 측정이 가능합니다.
분자 패킹은 다음을 사용하여 조사할 수 있습니다. 1매우 빠른 MAS에서 H NMR. 1D 170 kHz MAS에서 L-히스티딘(유사) 다형체의 H NMR 스펙트럼이 그림 5에 나와 있으며, 다른 패턴을 나타냅니다. 특히, 사방정계 형태(b)의 L-히스티딘은 단사정계 형태(c)와 다른 패턴을 나타냅니다. 이러한 차이는 다른 분자 패킹에서 비롯됩니다. 이것은 다음의 이점을 강조합니다. 1에 대한 H NMR 13이 두 가지 결정 형태를 식별하지 못하는 C CPMAS. 높은 풍부도(>99%) 및 Larmor 주파수(600T에서 14.1MHz) 덕분에 이러한 1D 스펙트럼을 관찰하는 데 XNUMX분도 채 걸리지 않습니다. 두 결정 형태의 차이는 다음을 관찰하여 확대할 수 있습니다. 1H/1분자간 민감도가 높아야 하는 H 동핵 상관 실험 1H/1H 연결성, 따라서 결정 패킹. 동핵 상관의 능력은 고유한 특징 중 하나입니다. 1높은 감도와 풍부함 덕분에 H NMR. 그림 6은 2D를 제공합니다. 1사방정계 및 단사정계 형태의 L-히스티딘의 H 이중 양자(DQ)/단일 양자(SQ) 동핵 상관 스펙트럼. 1D 스펙트럼은 로컬 정보만 표시하지만 2D 동핵 상관 스펙트럼은 중첩된 스펙트럼에 명확하게 표시된 것처럼 분자 패킹에 대한 정보도 반영합니다. DQ 일관성은 다음을 통해 생성됩니다. 1H-1H 쌍극자 상호 작용, 교차 피크 강도는 공간적 근접성을 반영합니다. 예를 들어, H1과 H4 사이의 핵간 거리는 사방 정계의 경우 4.1Å이고 단사 정계의 경우 훨씬 짧고 2.86Å입니다. 거리의 차이는 1.4배에 불과하지만 단사정계 형태의 쌍극자 상호작용은 2.9배 더 강하다. 따라서 H1-H4 상관관계는 단사정계 형태에서만 관찰됩니다. 2D 실험이지만 측정 시간은 일반적으로 XNUMX시간 미만이므로 보다 높은 처리량을 제공합니다. 13씨씨피마스.
1H/14N 상관 NMR은 유익한 정보도 제공합니다. L-히스티딘에는 여러 가지 가능한 양성자화 상태가 있습니다. 이미다졸 고리에 있는 τ 및 δ의 두 질소 중 하나 또는 둘 다 NH 부분으로 양성자화될 수 있습니다. 또한, L-히스티딘은 양성이온일 수 있다. 두 방법 모두 수소 위치에 민감하지 않기 때문에 XRD 또는 ED로 이러한 양성자화된 상태를 구별하는 것은 어렵습니다. 하지만, 1H/14L-히스티딘의 N 상관 스펙트럼(그림 7)은 명확한 답을 제공합니다. L-histidine·HCl·H의 산성 환경에서2O, XNUMX개의 NH 상관관계가 나타난다. 이것은 τ 및 δ 질소가 모두 양성자화되었음을 명확하게 보여줍니다. 하나 이상의 NH 상관 관계가 저주파 위치에 나타납니다. 14-260ppm에서 N 치수는 이 아미노산이 NH와 함께 양성이온임을 시사합니다.3+ 절반. 이것은 NH에서 작은 XNUMX극 결합 때문입니다.3+ 로컬 대칭으로 인해. 한편, XNUMX개의 L-히스티딘 다형체는 각각에 대해 XNUMX개의 NH 피크만 제공합니다. 둘 다 Zwitterion이고 τ 및 δ 질소 중 하나만 양성자화됨이 분명합니다. 유의해야 할 점은 1H/14N은 일반적으로 10분 미만이 소요됩니다. 1H 및 14N은 풍부한 핵입니다.
위의 모든 측정은 600 T에서 1 mm fast MAS ssNMR 프로브(JEOL RESONANCE Inc.)가 장착된 JNM-ECZ14.1R spectrometer(JEOL RESONANCE Inc., Japan)를 사용하여 수행되었습니다. 측정에 사용된 샘플 양은 각각 약 1 mg입니다. .
FIG.1
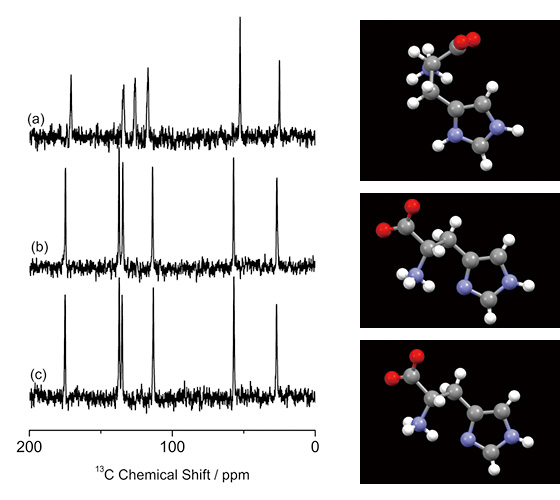
13(a) L-히스티딘·HCl·H의 C CPMAS 스펙트럼2O, (b) L-히스티딘(orthorhombic) 및 (c) L-histidine(monoclinic), 분자 형태와 함께. (a)에 대한 256개의 스캔과 (b) 및 (c)에 대한 512개의 스캔이 누적되었습니다. (a)는 JNM-ECA16.4II 분광기(JEOL RESONANCE Inc., Japan)를 사용하여 700 T에서 측정되었습니다. 그림은 참조 7에서 재현됩니다.
FIG.2

(a) TEM 이미지 및 (b) 미정질 L-히스티딘·HCl·H의 나노빔(직경 100 nm) 회절 패턴2오 샘플. 회절 패턴은 (a)에서 흰색 원으로 표시된 영역에서 얻어졌다. 그림은 참조 7에서 재현됩니다.
FIG.3
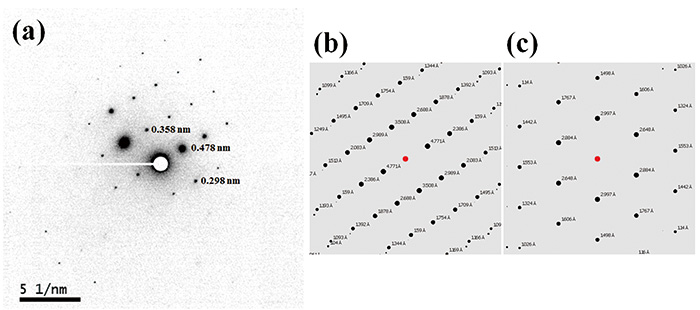
(a) L-히스티딘(orthorhombic)에 대해 부정적으로 표시된 실험적 ED 패턴 및 (b) L-histidine(orthorhombic) 및 (c) L-histidine(monoclinic)에 대해 계산된 ED 패턴. 회절 지점에 해당하는 d-간격은 보정된 카메라 길이 40cm 및 2.51kV 가속 전압에서 파장 200pm에 의해 추정됩니다. ED 패턴은 [631] 영역 축 입사 빔에 대해 계산되었습니다. 그림은 참조 7에서 재현됩니다.
FIG.4

(a) L-히스티딘(단사정계)에 대해 부정적으로 표시된 실험적 ED 패턴 및 (b) L-히스티딘(사방 정계) 및 (c) L-히스티딘(단사정계)에 대해 계산된 ED 패턴. 회절 지점에 해당하는 d-간격은 보정된 카메라 길이 40cm 및 2.51kV 가속 전압에서 파장 200pm에 의해 추정됩니다. ED 패턴은 [100] 구역 축 입사 빔에 대해 계산되었습니다. 그림은 참조 7에서 재현됩니다.
FIG.5
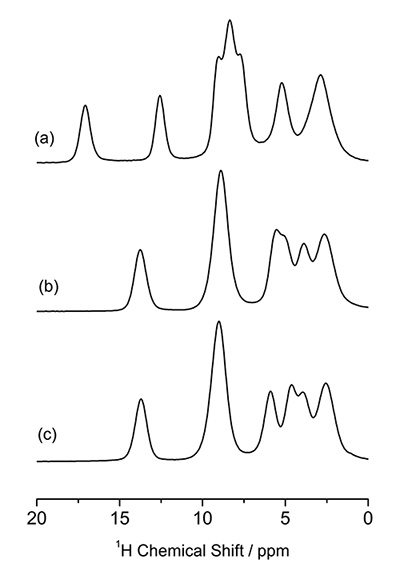
1(a) L-히스티딘·HCl·H의 H NMR 스펙트럼2O, (b) L-히스티딘(사방정계) 및 (c) L-히스티딘(단사정계). 그림은 참조 7에서 재현됩니다.
FIG.6
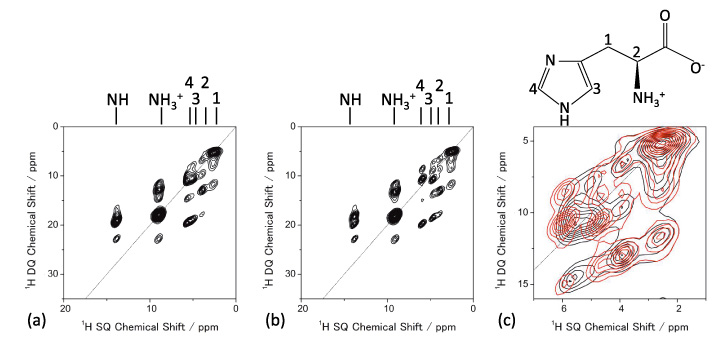
1H DQ/1(a) L-히스티딘(사방정계) 및 (b) L-히스티딘(단사정계)의 H SQ NMR 스펙트럼. 중첩된 스펙트럼의 확장은 (c)(검은색의 L-히스티딘(orthorhombic) 및 빨간색의 L-histidine(단사정계))에도 표시됩니다. 각 t에 대한 XNUMX개의 스캔1 기간은 32 t로 누적되었습니다.1 증분. 그림은 참조 7에서 재현됩니다.
FIG.7
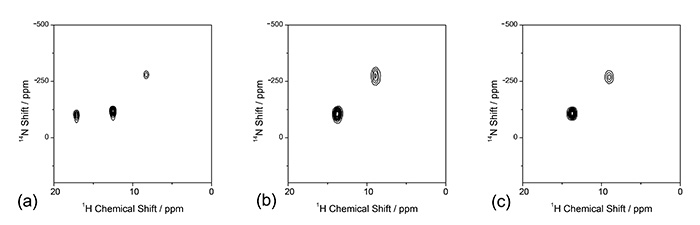
1시간/{14N} (a) L-히스티딘·HCl·H의 NMR 스펙트럼2O, (b) L-히스티딘(사방정계) 및 (c) L-히스티딘(단사정계). 스펙트럼(a)은 90mm HXMAS 프로브(JEOL RESONANCE Inc., 일본)를 사용하여 0.75kHz MAS 속도에서 측정되었습니다. 각 t에 대해 XNUMX개의 스캔1 기간은 (a) 64 및 (b)/(c) 32 t로 누적되었습니다.1 증분. 아니 1시간-14혼합 시간 동안 N 리커플링이 적용되었습니다. 그림은 참조 7에서 재현됩니다.
결정질 다형체를 위해 개발된 새로운 방법
화학, 약학, 재료 과학 등에서 질소의 중요성에도 불구하고 질소 NMR은 다소 제한적입니다. 이것은 단순히 감도가 낮기 때문입니다. 15낮은 존재비로 인한 N NMR 15엔(0.4%). 하지만 15N은 스핀 양자수가 I = 1/2이기 때문에 선호되며, 다른 동위 원소는 14N은 또한 99%의 유리한 높은 존재비를 갖는 NMR 활성 핵이다. 정수 스핀 양자수(I = 1)와 XNUMX중 극성 결합의 존재는 다음의 적용을 방해합니다. 14엔 NMR. 이러한 문제점을 극복하기 위해 개발한 1시간-{14N} 매우 빠른 MAS 조건에서 HMQC(heteronuclear multi-quantum coherence) 측정[8]. 이 방법을 사용하면 1mg 미만의 질량 제한 시료로 높은 처리량 측정이 가능합니다. 감도가 높기 때문에 방법을 XNUMX차원으로 확장할 수 있습니다. 14N/1H DQ/1H SQ 상관 실험[9]. 또한, 이 방법은 관찰을 탐구합니다. 35의약용 염[10]에서 종종 발견되는 Cl.
신호 할당은 그림 6에서 위에서 설명한 것처럼 NMR 스펙트럼을 해석하는 데 도움이 됩니다. XNUMX차원 동종/이핵 상관 관계가 XNUMX스핀 연결을 통해 신호를 할당하는 데 많은 도움이 되는 반면, XNUMX차원 실험은 훨씬 더 명확한 할당을 제공합니다. 이를 위해 개발한 13C/1H DQ/1로컬을 드러내는 HSQ 상관관계 1H-1부근의 H 스핀 네트워크 13다 [11]. 전체 과제는 자연적으로 풍부하게 존재하는 1mg 샘플을 사용하여 단일 XNUMX차원 스펙트럼에서 달성되었습니다.
염/공결정/연속체[12]
위에서 논의한 바와 같이 염/공결정/연속체의 식별은 XRD에서 수소를 찾을 수 있는 능력이 부족하기 때문에 제약 응용 분야에서 여전히 큰 문제로 남아 있습니다. 이 세 종류의 차이는 수소와 질소 사이의 거리 차이로 해석할 수 있습니다(그림 8). 따라서, 크기 1H-15핵간 거리의 세제곱에 반비례하는 N 쌍극자 상호작용은 소금/공결정/연속체에 대한 명확한 답을 제공해야 합니다.
여기서는 SCXRD와 ssNMR을 결합한 방법을 제안합니다. SCXRD가 전체 결정 구조를 결정하는 동안 ssNMR은 국지적인 핵간 거리를 제공합니다. 이 두 종류의 정보를 결합하여 결정 구조를 완벽하게 이해할 수 있습니다. 시연으로 먼저 그림 9에 표시된 10개의 모델 다중 구성 요소 시스템을 합성합니다. 결정 구조는 SCXRD에 의해 결정됩니다. 결과는 예상대로 N과 OH 사이의 분자간 접촉의 존재를 명확하게 보여줍니다(그림 1). 문제는 그것이 소금/공결정/연속체인지 여부입니다. 이 질문에 답하기 위해 SCXRD로 수소 위치를 결정하려고 시도했지만 기계 의존적 값을 제공하여 위치를 신뢰할 수 없습니다. SCXRD에 의해 결정된 결정 구조가 명확하게 보여주듯이 분자간 15H/XNUMXN 결합이 있습니다. 그만큼 1H/15N 거리, 따라서 사이의 결합 강도 1H 및 15N, 소금/공결정/연속체 문제에 대한 답을 제공해야 합니다. 예를 들어, 1H/15SA2의 N 거리는 1.25Å으로 결정됩니다(그림 10). SCXRD에 의해 결정되는 2.54Å의 질소와 산소 사이의 거리에서 수소가 산소와 질소의 중간에 위치하므로 SA2가 연속체라는 결론을 내릴 수 있습니다. SA2는 ΔpKa가 3보다 큰 강산과 염기로 구성된다는 점에 유의해야 합니다. 이 결과는 ΔpKa가 큰 시스템에서도 염/공결정/연속체를 식별하기 위한 SCXRD/ssNMR 측정의 중요성을 강조합니다. 다른 세 시스템의 구조와 핵간 거리는 성공적으로 결정되었습니다(그림 10). 이 방법의 병목 현상은 실험 시간입니다. 1H-15N 거리 측정. 자연적으로 존재하는 양이 적을 뿐만 아니라 15N과 작은 1H-15N 커플링, 이러한 제약 샘플은 일반적으로 매우 긴 1HT1 휴식 시간. 또한 빠른 MAS의 필요성으로 인해 샘플 양이 줄어들어 감도가 더욱 감소합니다. 우리는 다음 섹션에서 논의된 대로 처리량을 개선하는 방법을 개발했으며 각 측정에는 여전히 4-5일이 필요합니다. 처리량이 제한되어 있다는 사실에 동의합니다. 그럼에도 불구하고 우리는 이 방법이 다른 어떤 방법도 명확한 답을 주지 않기 때문에 상당히 유용하다고 생각합니다.
모든 NMR 측정은 700T에서 1mm 이중 공진 고속 MAS 프로브(JEOL RESONANCE Inc.)를 사용하는 JNM-ECA16.4II NMR 분광계(JEOL RESONANCE Inc.)로 수행되었습니다.
FIG.8
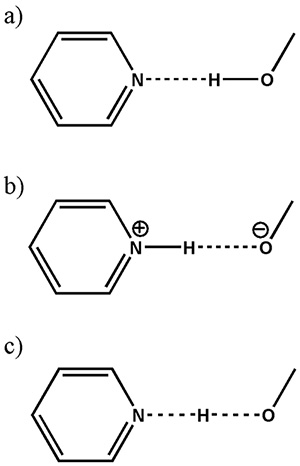
전형적인 O에서 (a) 공결정, (b) 염 및 (c) 연속체(H-원자 위치가 두 개의 중원자 사이에 공유됨)의 도식적 표현...H...N 상호 작용. 그림은 참조 12에서 재현됩니다.
FIG.9
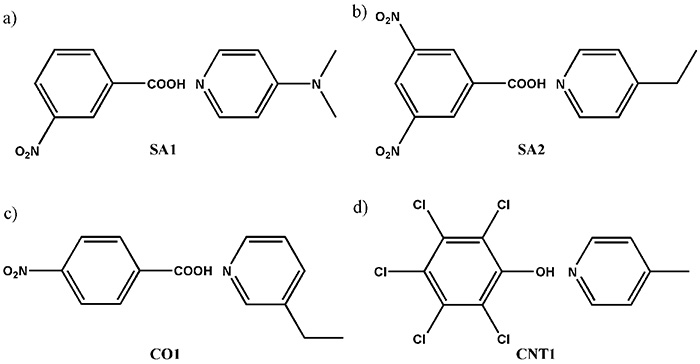
(a) SA1(3-니트로벤조산 및 N,N-디메틸피리딘-4-아민), (b) SA2(3,5-디니트로벤조산 및 4-에틸피리딘), (c) CO1(4-니트로벤조산 및 3-에틸피리딘) 및 (d) CNT1(펜타클로로페놀 및 4-메틸피리딘). 그림은 참조 12에서 재현됩니다.
FIG.10
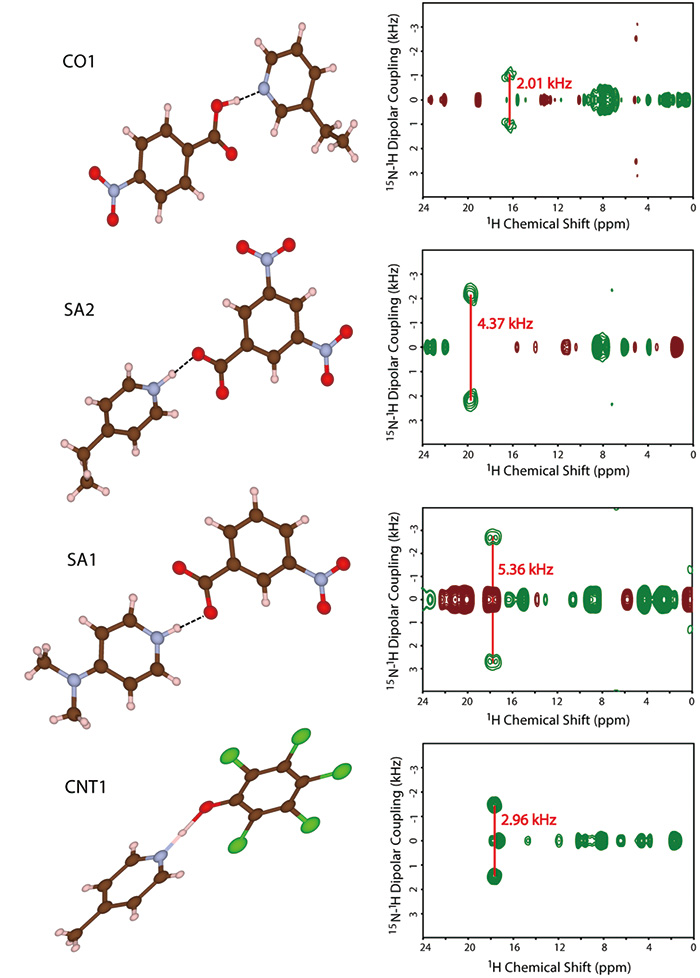
분자 구조 및 XNUMX차원 invCP-VC 스펙트럼(15N-1H 쌍극자 결합 대 1H 화학적 이동) SA1, SA2, CO1 및 CNT1. 그림은 참조 12에서 재현됩니다.
염/공결정/연속체를 위해 개발된 새로운 분석법
의 크기 1H/15N 쌍극자 결합은 정확하게 측정되어야 합니다. 그러나 1) 낮은 풍부성으로 인해 간단한 작업이 아닙니다. 15N(0.4%), 2) 작은 자이로자기 비율(1/10의 1H) 및 3) 풍부한 1결합되지 않은 H 핵 15N, 낮은 감도, 작은 쌍극자 결합(1-7kHz) 및 1각각 H 공명. 더 중요한 것은 이전 방법이 1H/15신뢰할 수 없는 거리를 제공하는 실험 조건에 따라 달라지는 N 쌍극자 결합. 이러한 어려움을 극복하기 위해 빠른 MAS에서 가변 접촉 시간(inv CP-VC) 방법이 있는 역검출 CP를 도입했습니다[13]. 첫째, 이 방법은 실험 조건에 독립적인 잘 정의된 쌍극자 분할을 제공합니다[14]. 실제로 inv CP-VC 방법의 스케일링 계수는 rf 필드 강도에 크게 의존합니다. 그러나 B가 있는 지역의 신호는1 불균일성은 넓은 스펙트럼 범위에 걸쳐 흩어져 있어 이러한 신호를 보이지 않게 만듭니다. 따라서 균질 B의 신호1 필드는 선택적으로 관찰됩니다. 에 의한 감도 향상 1inv CP-VC에서 H 검출은 적은 양과 시료량으로 인해 낮은 감도를 완화합니다. 실험적으로 inv CP-VC가 1H/152kHz의 N 커플링. inv CP-VC는 1H 공명, 선택적 관찰 제공 1H 부근 15N. 이것은 사이의 중첩된 공진의 복잡성을 피합니다. 1Hs. 또한 inv CP-VC는 1mg 미만의 질량 제한 시료를 분석하는 방법을 제시합니다.
스핀 시스템이 NMR 측정을 시작하기 전에 열 평형에 가깝게 돌아가도록 NMR 측정의 연속 스캔 사이에 반복 지연을 삽입해야 합니다. 반복 지연이 T 차수여야 하므로1 일반적으로 나머지 실험보다 훨씬 긴 이완 시간 T1 이완 시간은 NMR에서 실험 시간의 지배적인 요소입니다. inv CP-VC 실험에서 자화는 1따라서, 1HT1 중요하다. 그러나 잘 결정화된 저분자량 API는 매우 긴 경향이 있습니다. 1HT1 수십에서 수백 초의 이완 시간으로 처리량을 크게 줄입니다. 빠른 MAS 속도에서는 문제가 더 심각합니다. 1H-1H 스핀 확산이 억제되어 더 오래 지속됩니다. 1HT1 휴식 시간. 우리의 관심 대상인 NH 양성자는 다른 1H와 공간적으로 스펙트럼적으로 분리되어 있으므로 매우 느립니다. 1H-1H 스핀 확산은 1열 평형으로 회복하는 H 자화. 이로 인해 속도가 느려집니다. 1HT1 나머지 부분에 비해 NH 양성자의 이완 시간 1Hs. 이러한 어려움을 극복하기 위해 RFDR(Radio-Frequency Driven Recoupling) 시퀀스를 적용했습니다. 1H, 반복 지연 동안 [15]. 이것은 향상 1H-1H 스핀 확산, 빠르게 이완되는 자화를 가져옴 1H에서 NH 양성자로. 빠르게 이완되는 양성자의 이완 메커니즘을 여러 번 활용하기 때문에 NH 양성자뿐만 아니라 전반적인 감도도 향상될 수 있습니다. 우리는 또한 다음에 적합한 RFDR 시퀀스에서 위상 순환을 최적화했습니다. 1H 혼합 [16, 17].
결론
TEM과 NMR은 도입된 지 70년이 넘었음에도 불구하고 지금도 지속적으로 개선되고 있습니다. 최근 TEM에 도입된 고감도 카메라는 단일 입자 분석 접근법을 사용하여 단백질 구조를 결정하기 위해 cryo TEM의 새로운 응용 분야에 대한 길을 열어줍니다. 감도 향상은 단백질뿐만 아니라 저분자량 API를 포함한 빔에 민감한 시료에도 유용합니다. ssNMR의 빠른 MAS 기술에서 또 다른 큰 버스트가 관찰됩니다. 1H NMR 심지어 단단한 고체. 이러한 새로운 개발은 이전에는 접근할 수 없었던 새로운 정보를 제공할 뿐만 아니라 광범위한 사용을 위한 핵심 요소 중 하나인 처리량을 향상시킵니다. 또한 서로 보완적인 여러 가지 분석 방법을 적용하는 것이 매우 중요합니다. 적절한 조합은 높은 처리량으로 유용한 정보를 제공합니다. 실제로 JEOL Ltd.도 매력적인 장비 조합을 제공하기 위해 YOKOGUSHI 전략을 추진하고 있습니다.
이 기사에서는 XRD, ED 및 ssNMR을 결합하여 결정질 다형체 및 염/공결정/연속체 문제를 포함한 제약 과학의 구조적 문제를 해결합니다. 결정질 다형 문제의 경우 ED와 1PXRD를 보완하는 방법으로 결정 형태를 식별하기 위한 H 고속 MAS NMR 및 13씨씨피마스. ED는 나노 크기에서 마이크로 크기의 단결정까지 결정 형태를 결정할 수 있습니다. 반면에, 1H fast MAS는 분자 형태가 유사한 결정형을 구별할 수 있습니다. 또한 빠른 MAS는 1H/14질소 핵에 가까운 양성자 위치를 제공하는 N 상관 관계. 염/공결정/연속체를 식별하기 위해 매우 빠른 MAS 속도에서 SCXRD 및 ssNMR의 결합된 접근 방식이 도입되었습니다. SCXRD는 전체 분자 구조를 제공하지만 소금/공결정/연속체 문제에 중요한 양성자 위치를 결정하지 못합니다. 반면에 ssNMR은 정확한 1H-15N 거리, 전역 구조는 거의 얻지 못하지만. 이 접근법은 염/공결정/연속체 문제에 답하기 위해 결정 구조에서 수소 결합에 이르기까지 분자 구조에 대한 완벽한 이해를 제공합니다. ΔpKa > 3인 다성분 시스템에서 연속체의 형성은 SCXRD 및 ssNMR을 사용한 철저한 조사의 중요성을 강조합니다.
감사의
여기에 제시된 모든 작업은 RIKEN CLST-JEOL 협업 연구소에서 그룹 구성원과 함께 수행되었습니다. 모든 그룹 구성원과 JEOL Ltd. 및 JEOL RESONANCE Inc.의 큰 지원에 감사드립니다. 또한 방갈로르에 있는 인도 과학 연구소, AMES 연구실, 교토 대학, 도쿄 농업 기술 대학, 워릭 대학, 릴 대학, 미시간 대학의 유익한 협력에 감사드립니다.
참고자료
- RK 해리스, J. Pharm. 파마콜. 59 (2007) 225-239.
- M. Geppi, G. Mollica, S. Borsacchi, CA Veracini, 신청 분광학 신부님. 43 (2008) 202-302.
- FG Vogt, 퓨처메드 화학. 2 (2010) 915-921.
- Y. Nishiyama*, Natural Abundance 샘플을 위한 60-100kHz의 Fast Magic-Angle 샘플 회전 고체 NMR, 고체 핵 자기 공명, 78 (2016) 24-36. DOI: 10/j. ssnmr. 1016. 2016. 06.
- Y. Nishiyama*, 40 ‒ 120 kHz의 초고속 MAS 속도 하에서의 고체 NMR, NMR 분광학의 실험적 접근법 - 생명 과학 및 재료 과학에 대한 방법론 및 응용, Springer(2017).
- T. Kobayashi, Y. Nishiyama*, M. Pruski*, 역검출을 통한 Heteronuclear 상관 분광법, 고체 상태 NMR의 현대적 방법: 실무자 가이드, 왕립 화학회(2018).
- T. Oikawa, M. Okumura, T. Kimura, Y. Nishiyama*, 전자 회절을 충족하는 고체 NMR: 작은 유기 미정질 샘플의 결정 다형 결정, 액타 크리스탈. C73 (2017) 219-228. DOI: 10. 1107/S2053229617003084.
- Y. 니시야마*, Y. 엔도, T. 네모토, H. 우츠미, K. 야마우치,
